?約翰·霍普金斯大學(xué)的研究團(tuán)隊(duì)最近研發(fā)了一種早期腫瘤篩查方法����,可以同時(shí)檢測(cè)出8種腫瘤。Credit:ElizabethCook與KaitlinLindsay制圖。撰文|王承志責(zé)編|陳曉雪知識(shí)分子為更好的智趣生活I(lǐng)D:The-Intellec
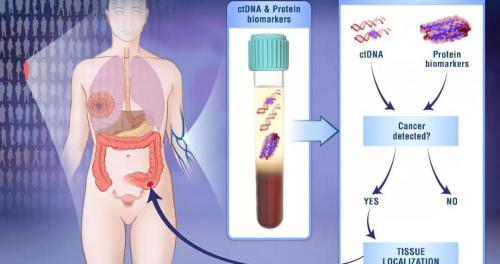
?約翰·霍普金斯大學(xué)的研究團(tuán)隊(duì)最近研發(fā)了一種早期腫瘤篩查方法��,可以同時(shí)檢測(cè)出8種腫瘤�����。Credit: Elizabeth Cook與Kaitlin Lindsay制圖�。
撰文 | 王承志
責(zé)編 | 陳曉雪
知識(shí)分子為更好的智趣生活 ID:The-Intellectual
●●●
腫瘤是目前對(duì)人類威脅最大的疾病之一��。如果不發(fā)生轉(zhuǎn)移,大部分實(shí)體腫瘤可以通過(guò)手術(shù)切除完全治愈�����。一旦腫瘤發(fā)生轉(zhuǎn)移,僅靠手術(shù)通常無(wú)濟(jì)于事�����。
實(shí)際上��,很多成人的腫瘤從初期病變發(fā)展到晚期要經(jīng)歷長(zhǎng)達(dá)20-30年的時(shí)間。如何在早期檢測(cè)到腫瘤��,特別是在影像學(xué)能檢測(cè)到腫瘤之前發(fā)現(xiàn)病變���,是醫(yī)學(xué)界的一個(gè)重要的研究方向����。
目前唯一廣泛使用的腫瘤早期篩查技術(shù)是前列腺癌特異抗原(PSA����,一種激肽酶家族蛋白���,正常人血漿中含量極低���,常用于作為前列腺癌患者的生物標(biāo)志物)��,然而這種檢測(cè)技術(shù)的特異性還存在較大爭(zhēng)議�����。目前臨床常用的其它腫瘤早篩項(xiàng)目通常是侵入性或放射性的�����,例如結(jié)腸鏡和乳腺X線檢查���。而無(wú)創(chuàng)檢查如血檢的高假陽(yáng)性率使得很多健康人得到“陽(yáng)性”結(jié)果而承受巨大的心理壓力和焦慮����。
近年來(lái),基于基因測(cè)序的血檢(也就是通常所說(shuō)的“液體活檢”,是一種非侵入式的血液測(cè)試)給腫瘤早篩帶來(lái)了新的希望���,因?yàn)檫@種方法通常檢測(cè)“驅(qū)動(dòng)”基因的突變(導(dǎo)致腫瘤的關(guān)鍵突變)�,而這些突變通常只發(fā)生于異常增殖的細(xì)胞����。
液體活檢兼具無(wú)創(chuàng)和特異性高的優(yōu)點(diǎn)����,但是,目前也面臨幾個(gè)重大的挑戰(zhàn):
1. 對(duì)于早期腫瘤檢測(cè)靈敏度還不夠����。早期腫瘤每毫升血清含有的致病突變常少于1個(gè)拷貝����,這低于目前液體活檢檢測(cè)范圍的下限[1, 2]。
2. 液體活檢迄今為止還沒(méi)有大規(guī)模的健康對(duì)照人群實(shí)驗(yàn)�,而這對(duì)特異性的評(píng)估很關(guān)鍵 [3]。
3. 液體活檢無(wú)法分辨出致病突變的來(lái)源。在影像學(xué)不能檢出的早期階段,確定腫瘤來(lái)源是非常重要的。
針對(duì)液體活檢靈敏度較低的問(wèn)題����,約翰·霍普金斯大學(xué)醫(yī)學(xué)院Bert Vogelstein和Anne Marie Lennon研究組去年開(kāi)發(fā)了聯(lián)合使用ctDNA KRAS基因檢測(cè)和四種蛋白生物標(biāo)志物的方法,將早期胰腺癌的檢出率提升到接近2/3 �,這種方法的靈敏度超過(guò)了以往任何單個(gè)指標(biāo)[2]。
最近�����,這兩個(gè)研究組和約翰·霍普金斯大學(xué)的其它三個(gè)研究組(Cristian Tomasetti�,Kenneth W. Kinzler 和 Nickolas Papadopoulos研究組)一起拓展了這種方法:聯(lián)合應(yīng)用液體活檢和蛋白腫瘤標(biāo)志物檢測(cè)��,可以一次檢測(cè)8種不同的早期腫瘤 [4]�����。1月19日的《科學(xué)》(Science)在線發(fā)表了這一最新研究成果��。
這項(xiàng)研究的第一個(gè)難點(diǎn)是�,需要設(shè)計(jì)一個(gè)能夠覆蓋大多數(shù)腫瘤常見(jiàn)驅(qū)動(dòng)突變的基因位點(diǎn)集合(Panel)用于擴(kuò)增(PCR)���。首先����,這個(gè)集合需要足夠多的位點(diǎn)來(lái)覆蓋多種腫瘤�,但是當(dāng)位點(diǎn)增多時(shí)也會(huì)增加擴(kuò)增等操作引起的人為突變���,從而降低信噪比。其次���,檢測(cè)位點(diǎn)增多時(shí)會(huì)在相同數(shù)據(jù)量情況下降低測(cè)序深度����,而低頻突變需要足夠的深度才能被檢測(cè)到。最后,作為一項(xiàng)需要用于臨床的技術(shù),成本也是必須考慮的因素��,過(guò)多的檢測(cè)位點(diǎn)將增加患者的負(fù)擔(dān)�����。因此����,需要平衡檢測(cè)的廣度和深度���,找到合適的基因位點(diǎn)集合��。
研究人員使用已公開(kāi)發(fā)表的數(shù)據(jù)進(jìn)行模擬分析,發(fā)現(xiàn)當(dāng)擴(kuò)增位點(diǎn)超過(guò)60個(gè)時(shí),繼續(xù)增加擴(kuò)增位點(diǎn)不能擴(kuò)大所檢測(cè)的腫瘤范圍���,并且會(huì)增加假陽(yáng)性率(圖1)?;诖耍芯咳藛T設(shè)計(jì)了一個(gè)包含61個(gè)擴(kuò)增位點(diǎn)的集合����,并對(duì)805位腫瘤病人使用了這個(gè)集合進(jìn)行了檢測(cè)�,發(fā)現(xiàn)了在82%的病人中可以檢測(cè)到至少一個(gè)突變位點(diǎn)�。
?圖1:腫瘤特異突變擴(kuò)增的測(cè)試。圖片來(lái)源:Cohen JD et al., Science (2018)
之前的研究顯示,聯(lián)合使用血漿蛋白腫瘤標(biāo)志物可以提高ctDNA的檢測(cè)效率。研究人員通過(guò)文獻(xiàn)搜索���,篩選了已知的敏感性大于10%�����,特異性大于99%的41種腫瘤標(biāo)志物�����。通過(guò)對(duì)腫瘤病人和健康對(duì)照人群的血漿的實(shí)際測(cè)試,研究人員最終篩選出8種能夠很好地區(qū)分腫瘤病人和健康人群的標(biāo)志物����。值得一提的是���,在這項(xiàng)測(cè)試中�,研究人員選擇了免疫檢測(cè)(即使用標(biāo)志物特異的抗體)而非昂貴的質(zhì)譜檢測(cè),充分保證了臨床可行性。
研究人員將這種結(jié)合ctDNA和腫瘤標(biāo)志物的檢測(cè)方法稱為CancerSEEK�,并用這種方法對(duì)1005位已經(jīng)診斷出I期和II期的腫瘤病人(I期和II期屬于早期)進(jìn)行了測(cè)試,這些病人包括了最常見(jiàn)的8種腫瘤:卵巢癌�,肝癌,胃癌,胰腺癌����,食道癌,腸癌,肺癌和乳腺癌。
實(shí)驗(yàn)顯示CancerSEEK對(duì)8種腫瘤檢測(cè)靈敏度的中位數(shù)達(dá)到了70%����,其中對(duì)卵巢癌的靈敏度超過(guò)了98%。即使在如此高的靈敏度條件下�����,總體特異性也超過(guò)99%。特別值得注意的是����,CancerSEEK對(duì)早期腫瘤具有很高的靈敏度���,對(duì)實(shí)驗(yàn)樣本的統(tǒng)計(jì)中最早期的I期肝癌甚至達(dá)到了驚人的100%�。
液體活檢目前還無(wú)法檢測(cè)腫瘤來(lái)源��,限制了其應(yīng)用范圍����。研究人員利用CancerSEEK的臨床測(cè)試的結(jié)果����,采用了一種有監(jiān)督的機(jī)器學(xué)習(xí)算法�����,將CancerSEEK結(jié)果與病人臨床檢測(cè)的結(jié)果匹配�����。結(jié)果顯示��,算法經(jīng)過(guò)學(xué)習(xí),即使在沒(méi)有任何臨床信息的情況下��,也能對(duì)腫瘤來(lái)源做出預(yù)測(cè)����。在有兩個(gè)候選器官時(shí)��,準(zhǔn)確率的中位數(shù)達(dá)到了83%�����,其中對(duì)腸癌和卵巢癌的準(zhǔn)確率分別達(dá)到100%和92%。在定位到單個(gè)器官時(shí)��,總準(zhǔn)確預(yù)測(cè)的中位數(shù)也達(dá)到了63%���。
?圖2:機(jī)器學(xué)習(xí)對(duì)腫瘤來(lái)源的預(yù)測(cè)�����。來(lái)源:Cohen JD et al., Science (2018)
研究人員稱�����,這種檢測(cè)的單次總成本不超過(guò)500美元。通過(guò)一次檢查,可以檢測(cè)至少8種早期腫瘤,并且大多數(shù)情況下可以追述腫瘤來(lái)源�����。如果在接下來(lái)的臨床實(shí)驗(yàn)中可以取得同等或更優(yōu)的效果�����,這種檢測(cè)方法可能修改目前早期腫瘤檢測(cè)的范式����,并將液體活檢的應(yīng)用推廣到新的高度�����。
不過(guò)��,一些研究液體活檢的科學(xué)家認(rèn)為�,使用這一通用的驗(yàn)血方法是否能夠減少癌癥患者的死亡而不會(huì)造成傷害�,還需要時(shí)間去發(fā)現(xiàn)�����。在《科學(xué)》的新聞報(bào)道中�,劍橋大學(xué)的癌癥研究員Nitzan Rosenfeld評(píng)論說(shuō)����,這是一個(gè)令人激動(dòng)的進(jìn)展���,“但在現(xiàn)實(shí)世界的評(píng)估將是一個(gè)漫長(zhǎng)的過(guò)程”[5]���。
參考文獻(xiàn):
1. Bettegowda C, Sausen M, Leary RJ, et al.:Detection of circulating tumor DNA in early- and late-stage human malignancies.Sci Transl Med 6: 224ra224, 2014.
2. Cohen JD, Javed AA, Thoburn C, et al.: Combined circulating tumor DNAand protein biomarker-based liquid biopsy for the earlier detection ofpancreatic cancers. Proc Natl Acad Sci US A 114: 10202-10207, 2017.
3. Cree IA, Uttley L, Buckley Woods H, et al.: The evidence base forcirculating tumour DNA blood-based biomarkers for the early detection ofcancer: a systematic mapping review. BMCCancer 17: 697, 2017.
4. Cohen JD, Li L, Wang Y et al.: Detection and localization of surgically resectable cancerswith a multi-analyte blood test. Science aar3247, 2018.
http://science.sciencemag.org/cgi/doi/10.1126/science.aar3247
5. Kaiser J.: ‘Liquid biopsy’ for cancer promises early detection. Science 359:6373, 2018.
制版編輯: 斯嘉麗|
本頁(yè)刊發(fā)內(nèi)容未經(jīng)書(shū)面許可禁止轉(zhuǎn)載及使用
公眾號(hào)、報(bào)刊等轉(zhuǎn)載請(qǐng)聯(lián)系授權(quán)
copyright@zhishifenzi.com
知識(shí)分子為更好的智趣生活 ID:The-Intellectual

